近日,中国科学院武汉病毒研究所陈建军研究团队在《ACS Nano》期刊发表了题为“Epitope-Optimized Influenza Hemagglutinin Nanoparticle Vaccine Provides Broad Cross-Reactive Immunity against H9N2 Influenza Virus”的研究论文。该研究成功开发出一种针对H9N2流感病毒的表位优化型纳米颗粒疫苗,在动物模型中展现出对多种H9N2毒株的广谱交叉免疫保护效力,为全球 H9N2 流感疫情的防控提供了创新性解决方案。
H9N2流感病毒在家禽中广泛流行,对全球家禽养殖业造成了严重的经济损失。自2020年以来,人类感染H9N2病例频发,部分毒株已进化出结合人类唾液酸受体的能力,凸显跨物种传播风险。此外,持续的抗原漂移削弱了现有疫苗的保护效力,因此,开发诱导广谱免疫反应的通用型疫苗迫在眉睫。
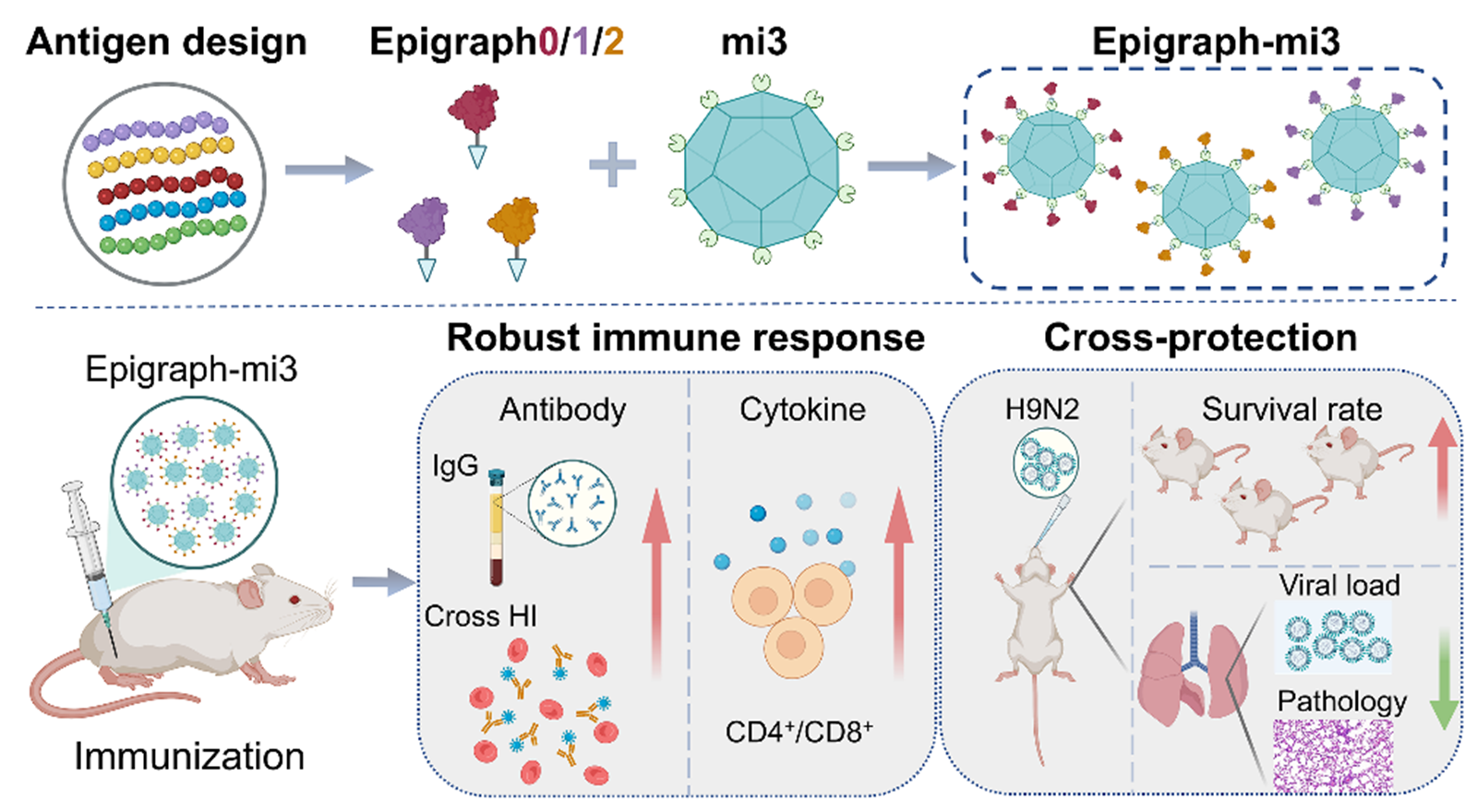
为应对这一挑战,研究团队整合了GISAID数据库中所有H9N2毒株血凝素(HA)氨基酸序列作为数据集,并运用一种基于图论的潜在表位最大化的算法加以处理,设计了三条优化的H9 HA1抗原。该算法计算出的表位优化型抗原,理论上可最大化覆盖所有H9毒株HA蛋白的潜在T细胞表位。为弥补亚单位疫苗免疫原性不足的缺陷,研究团队又将三条优化抗原与mi3纳米(一种由60个相同的亚基自组装成的正十二面体纳米颗粒蛋白)递送载体结合,成功制备出H9N2通用型纳米疫苗,并验证该疫苗具有良好的热稳定性。
动物实验结果显示,该疫苗在小鼠体内有效诱导了针对14株不同分支的H9N2代表性毒株的高水平交叉反应抗体,并大幅度激活了CD4+和CD8+ T细胞免疫反应。此外,它对3株代表性H9N2毒株的致死性攻毒均提供了有效保护,免疫小鼠体重丢失较小,且存活率均可达到100%,肺部病毒载量也显著降低。表明该疫苗具备应对病毒变异的潜力。
该研究不仅为开发通用H9N2流感疫苗提供了新的思路和方法,还展示了该算法在疫苗设计中的强大应用潜力。本研究中H9N2候选疫苗的成功开发,有望在应对H9N2病毒的流行和防控方面发挥重要作用。研究团队未来将继续优化其广谱性,并拓展不同疫苗形式如灭活疫苗及mRNA疫苗的应用,以期为H9N2流感疫情防控提供更有力的科学支持。
武汉病毒所博士研究生郝梦婵为该论文的第一作者,陈建军研究员和张源副研究员为该论文的通讯作者。该研究得到了国家自然科学基金、国家重点研发计划以及广州国家实验室重大项目的资助。
论文链接:https://pubs.acs.org/doi/10.1021/acsnano.5c03199
 附件下载:
附件下载:
科学研究