原核生物(细菌和古菌)在和噬菌体长期的竞争过程中进化出丰富多样的抗病毒系统,这些系统可以通过切割或者修饰核酸物质,或消耗原核生物生长必需的代谢物来实现抗病毒目的。针对原核生物抗病毒免疫系统的研究不但能够促进我们对于抗病毒免疫系统的功能、起源和进化的理解,还能推动基于这些免疫系统开发出重要的生物学工具。近年来,中国科学院武汉病毒研究所邓增钦团队和合作团队揭示了包括NADase/Ago和III-E 型CRISPR-Cas7-11等多个原核生物免疫系统的分子机制(Cell Research 2023,Nature Microbiology 2022,Nucleic Acids Research 2022)。DUF4297-HerA是近期发现的一种细菌新型抗病毒系统,其中DUF4297蛋白可能具有核酸酶活性;HerA广泛存在于原核生物中,其和存在于细菌、古菌和真核细胞中的AAA+ 蛋白一样形成寡聚体,利用水解ATP产生的能量驱动各种生物过程。近日,邓增钦团队在学术期刊Cell Research发表题为“Molecular and structural basis of an ATPase-nuclease dual-enzyme anti-phage defense complex”的研究论文。该研究通过解析一系列高分辨率的冷冻电镜结构并结合体外生化实验和抗噬菌体功能实验,揭示了具有双酶活性的DUF4297-HerA复合物的组装、酶活调控以及发挥抗病毒作用的分子机制。
研究团队首先发现DUF4297单独表达时形成尾对尾的二聚体,HerA形成螺旋状六聚体,两个蛋白分别表现出非常低的核酸酶和ATP水解酶活性。DUF4297和HerA共表达时会组装成一个大小约为1 MDa的巨大复合物,含有6个HerA分子和12个DUF4297分子。12个DUF4297蛋白分子排列成上下两层,其中仅下层DUF4297分子和HerA发生相互作用(图1a-b)。通过结构分析和功能验证证明不同蛋白分子之间形成的相互作用对于稳定复合物的形成和抗病毒功能都很重要。复合物的形成促使位于上层的DUF4297的核酸酶结构域二聚化(图1c),同时HerA构象发生改变使位于HerA蛋白亚基作用界面间的ATP水解酶活性位点处于高活性构象。这两个重要的蛋白构象变化使DUF4297和HerA都处于高酶活性状态。激活后的DUF4297-HerA复合物特异性切割双链DNA,而不切割单链DNA、单链RNA或双链RNA。
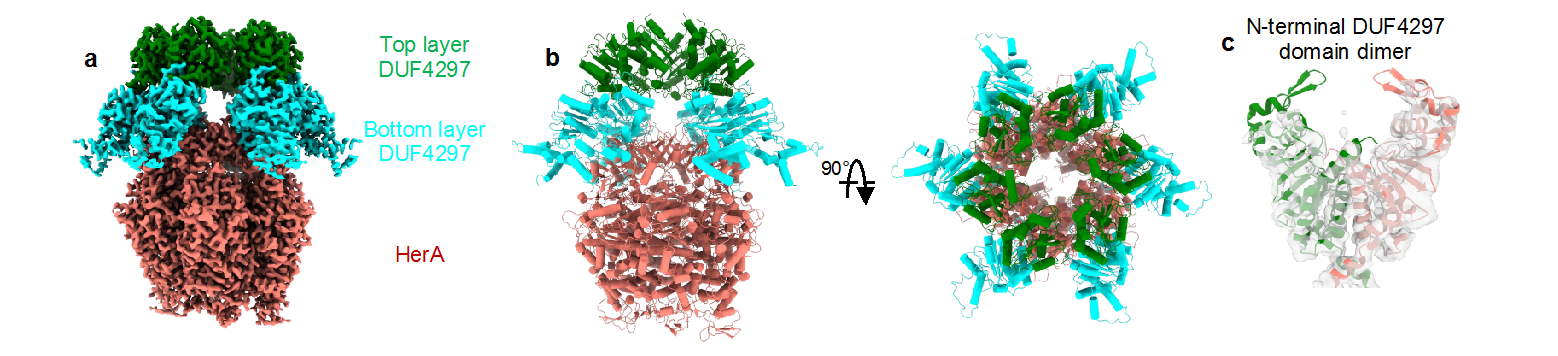
图1.DUF4297-HerA复合物
为了探究DUF4297和HerA是如何抵抗噬菌体感染的,研究团队检测了不同MOI值感染条件下细菌的生长情况。在低MOI条件下细菌虽然生长减缓,但最终能够恢复正常生长,而在高MOI时细菌死亡,说明DUF4297-HerA通过顿挫感染机制抵抗病毒感染。随后研究团队利用荧光显微镜观察到噬菌体感染后细菌细胞内的双链DNA发生降解形成空泡细胞(图2a,白色箭头所指为DNA发生降解形成空泡细胞)。有趣的是,虽然DUF4297-HerA复合物的核酸酶和ATP水解酶活性在互不影响,但突变失活其中任一酶活性都会使该系统的抗病毒功能丧失,说明核酸酶和ATP水解酶需协同作用发挥抗病毒功能,其具体机制还有待进一步研究(图2)。
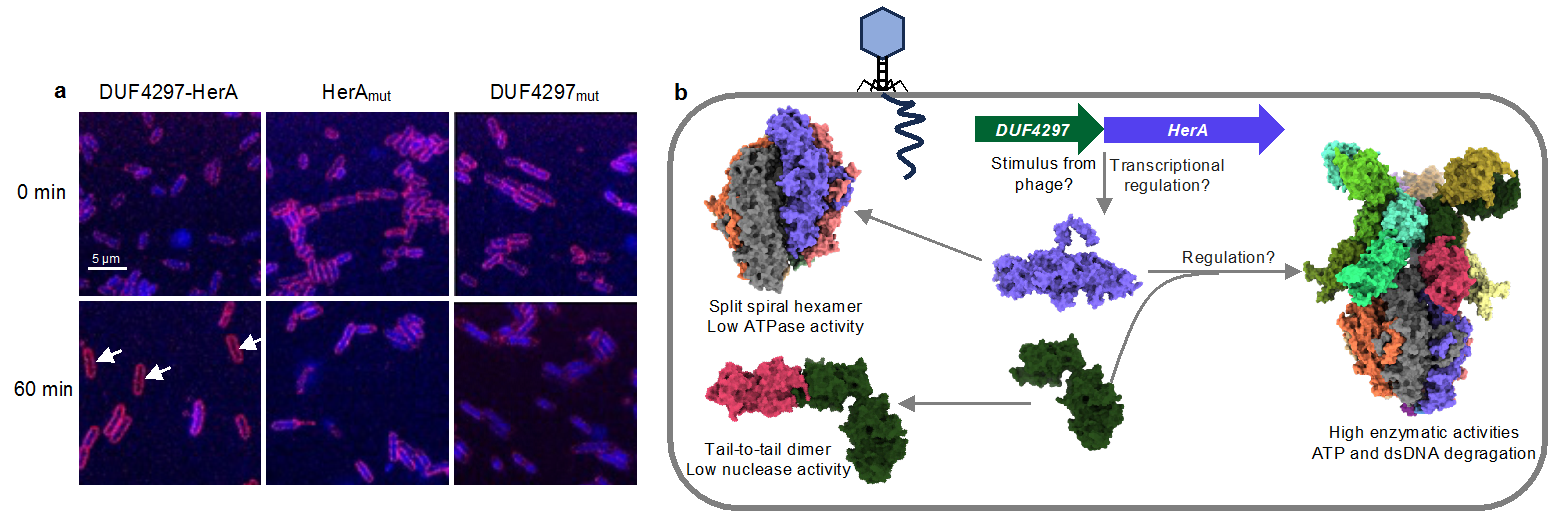
图2. DUF4297-HerA系统作用模式图
此外,研究团队解析了HerA结合DNA以及ATP类似物处于多种功能状态下的复合物结构,为理解HerA及其同源蛋白如何通过水解ATP驱动HerA在DNA双链上运动提供了深入的结构见解。
武汉病毒所邓增钦研究员为该论文的通讯作者。武汉病毒所博士生安启银、王咏、田振华和天津医科大学韩洁博士为该论文的共同第一作者。该工作得到了天津医科大学张恒教授、福建医科大学温彦丞副教授和武汉大学赵海艳研究员的大力支持。
 附件下载:
附件下载:
科学研究