近日,中国科学院武汉病毒研究所/高致病性病毒与生物安全全国重点实验室王延轶研究员团队在国际知名学术期刊Proceedings of the National Academy of Sciences(PNAS)上发表了题为“SPNS1 is an essential cellular factor for EV-A71 by acting as a transporter of viral pocket factor”的研究论文。该研究首次揭示,宿主细胞内的溶酶体膜蛋白SPNS1能够作为病毒“口袋因子”的转运体,介导其释放,从而启动病毒脱壳过程。这一发现为阐明肠道病毒感染的关键机制提供了全新视角,也为防治手足口病等疾病提示了潜在的新型药物靶点。
肠道病毒71型(EV-A71)是引发儿童手足口病的主要病原体,严重感染可累及神经系统。病毒成功入侵细胞的核心步骤之一在于将其基因组RNA释放至细胞质,此过程称为“脱壳”。研究表明,EV-A71病毒颗粒内部存在被称为“口袋因子”的鞘脂类分子,该分子对于维持病毒结构的稳定至关重要。在感染后,口袋因子需在溶酶体中被移除,以触发病毒结构蛋白解离并释放RNA。然而,口袋因子自溶酶体中被移除后的具体转运机制,长期以来尚不明确。
研究团队利用CRISPR-Cas9策略,系统筛选支持EV-A71感染的宿主关键因子,鉴定溶酶体膜蛋白SPNS1为EV-A71的重要宿主因子。SPNS1是一种已知的溶酶体脂质转运蛋白,负责将如溶血磷脂等脂类分子从溶酶体腔转运至细胞质。研究人员发现,在SPNS1基因敲除的细胞中,EV-A71的感染被显著抑制。为深入阐明其作用分子机制,研究人员用叠氮标记了EV-A71病毒的口袋因子,并基于点击化学—铜离子催化的叠氮-炔烃环加成反应(CuAAC)追踪口袋因子的位置。在正常细胞中,病毒感染后,口袋因子从溶酶体内转移并扩散至细胞质,标志着口袋因子的成功释放与转运。而在SPNS1缺陷的细胞中,口袋因子则始终局限于溶酶体中,病毒脱壳过程受阻,这直接证实了SPNS1是口袋因子溶酶体转运的关键执行者。此外,SPNS1的转运活性依赖于溶酶体的酸性环境。进一步研究表明,SPNS1通过其跨膜螺旋形成的特异性结构域识别并结合口袋因子。SPNS1的特定关键氨基酸残基(如R76和H427)对其转运功能至关重要,这些位点的突变会使SPNS1丧失支持病毒感染的能力。
武汉病毒所青年研究员付玉志、博士研究生骆芳芳和杨柳为论文共同第一作者;王延轶研究员为论文通讯作者;中国疾病预防控制中心张勇研究员等为合作作者。该研究得到了国家重点研发计划、国家自然科学基金和中国科学院青促会等项目的资助。
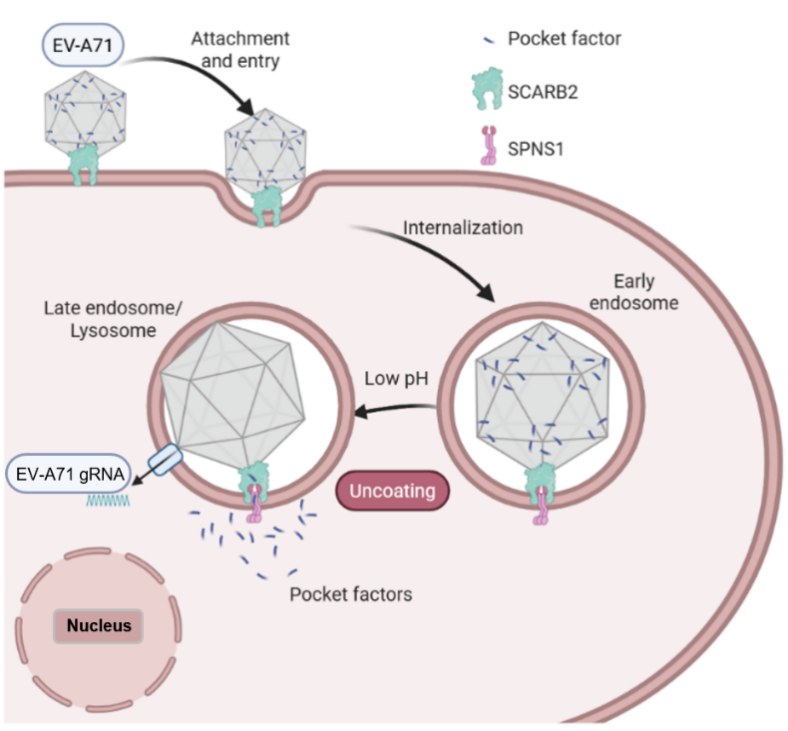
图1.SPNS1介导EV-A71“口袋因子”释放模式图
 附件下载:
附件下载:
科学研究