近日,中国科学院武汉病毒研究所周溪/任玉洁团队在国际学术期刊Cell Reports Medicine上发表了题为“Herpes simplex virus-1 encodes a STING antagonist that can be therapeutically targeted”的研究论文。该研究首次揭示了疱疹病毒1型(HSV-1)编码的UL38蛋白通过拮抗宿主STING信号通路逃逸免疫反应的分子机制,并基于该机制开发了一种靶向UL38-STING互作界面的多肽药物L4P,在动物感染模型中展现出显著的抗病毒效果,为HSV-1及相关疾病的治疗提供了新策略。
HSV-1是一种广泛感染人类的病原体,可引发口唇疱疹、角膜炎、脑炎等严重疾病,全球约38亿人感染。现有抗病毒药物(如阿昔洛韦)通过抑制病毒DNA聚合酶发挥作用,但耐药性问题日益突出。宿主先天免疫中的cGAS-STING通路是抵御DNA病毒的关键防线,而目前已报道HSV-1通过多种病毒蛋白(如ICP27、UL41等)逃逸该通路。然而,靶向疱疹病毒免疫逃逸机制的新型疗法仍鲜有报道。
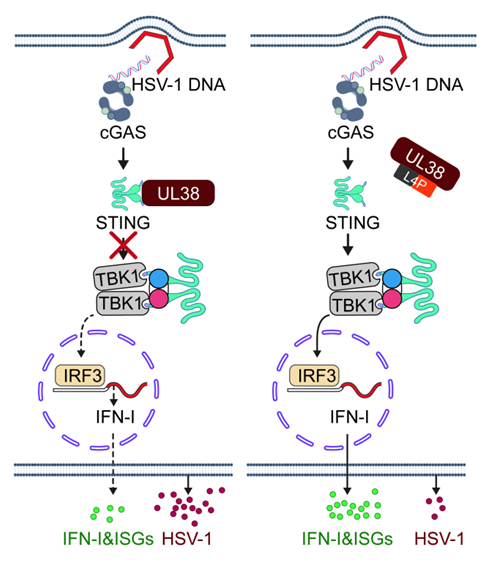
研究团队发现,HSV-1的衣壳蛋白UL38通过直接结合STING,阻断cGAMP与STING的结合,并抑制STING-TBK1-IRF3复合物的形成,从而拮抗干扰素及下游抗病毒基因的表达。通过构建UL38关键结构域缺失的突变病毒(HSV-1UL38Δ81-90),团队证实该突变病毒因无法抑制STING信号导致复制能力和致病性的显著降低。进一步,研究基于宿主STING上与UL38结合的序列,研究团队设计了一系列靶向STING-UL38互用界面的多肽。其中多肽L4P可特异性破坏UL38-STING互作,恢复STING介导的免疫应答,在细胞和动物模型中均展现出与阿昔洛韦相当的抗病毒效果,且具有良好的细胞和体内安全性。同时,L4P破坏的是病毒对天然免疫的抑制,而非激活额外的免疫;因此,随着对HSV-1的抑制,L4P不会继续上调免疫引发炎症等“副作用”。更有趣的是,L4P基于宿主STING蛋白序列设计,通过“解锁”病毒抑制的宿主免疫反应实现抗病毒效果,从理论上规避了病毒产生耐药突变的可能 - 如果HSV-1 UL38产生了不与L4P结合的突变,它同时就失去了结合STING拮抗宿主免疫的能力,这一药物设计新思路也为其他抗病毒药物的研发提供了启示。同时,基于该研究已申请国家发明专利1项。
武汉病毒所博士研究生王岸为该论文第一作者,周溪研究员和任玉洁青年研究员为共同通讯作者。该研究获得了国家重点研发计划和国家自然科学基金等项目的资助。
论文链接:https://www.cell.com/cell-reports-medicine/fulltext/S2666-3791(25)00124-7
 附件下载:
附件下载:
科学研究